

Las aminas son parte de los alcaloides que son compuestos complejos que se encuentran en las plantas. Algunos de ellos son la morfina y la nicotina. Algunas aminas son biológicamente importantes como la adrenalina y la noradrenalina. Las aminas secundarias que se encuentran en las carnes y los pescados o en el humo del tabaco.
Estas aminas pueden reaccionar con los nitritos presentes en conservantes empleados en la alimentación y en plantas, procedentes del uso de fertilizantes, originando N-nitrosoaminas secundarias, que son carcinógenas.
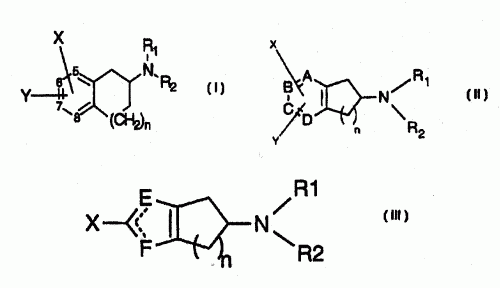 Como base de entendimiento es indispensable tener claro los conceptos básicos que son manejados en este tema, entre ellos podemos encontrar:
Como base de entendimiento es indispensable tener claro los conceptos básicos que son manejados en este tema, entre ellos podemos encontrar:Aminas: Las aminas son compuestos químicos orgánicos que se consideran como derivados del amoniaco y resultan de la sustitución de los hidrógenos de la molécula por los radicales alquilo.
Electrón: Se conoce como electrón a la partícula elemental

Hibridación: En química, se habla de Hibridación cuando en un átomo, se mezcla el orden de los electrones entre orbitales creando una configuración electrónica nueva.
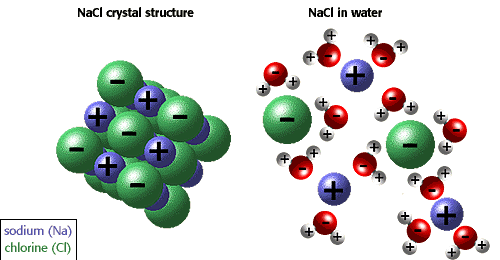
Polaridad: La polaridad química o sólo polaridad es una propiedad de las moléculas que representa la separación de las cargas eléctricas en la misma.
A continuación un video de las Aminas:
Aminas. ¿Dónde se encuentran?Las aminas se encuentran formando parte de la naturaleza, en los aminoácidos que conforman las proteínas que son un componente esencial del organismo de los seres vivos. Al degradarse las proteínas se descomponen en distintas aminas, como cadaverina y putrescina entre otras. Las cuales emiten olor desagradable. Es por ello que cuando la carne de aves, pescado y res no es preservada mediante refrigeración, los microorganismos que se encuentran en ella degradan las proteínas en aminas y se produce un olor desagradable.
Propiedades de la Aminas:
Las aminas son compuestos orgánicos derivados del amoniaco (NH3), y son producto de la sustitución de los hidrógenos que componen al amoniaco por grupos alquilo o arilo, se clasifican de acuerdo al número de sustituyentes unidos al nitrógeno en aminas primarias, aminas secundarias y terciarias.
Existen dos clases de propiedades:
Existen dos clases de propiedades:
PROPIEDADES FÍSICAS:
| Las aminas presentan puntos de fusión y ebullición más bajos que los alcoholes. Así, la etilamina hierve a 17ºC, mientras que el punto de ebullición del etanol es de 78ºC. CH3CH2OH P.eb. = 78ºC CH3CH2NH2 P. eb. = 17ºC La menor electronegatividad del nitrógeno, comparada con la del oxígeno, hace que los puentes de hidrógeno que forman las aminas sean más débiles que los formados por los alcoholes. También se observa que las aminas primarias tienen mayores puntos de ebullición que las secundarias y estas a su vez mayores que las terciarias. 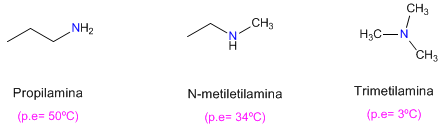 La amina terciaria no puede formar puentes de hidrógeno (carece de hidrógeno sobre el nitrógeno), lo que explica su bajo punto de ebullición. En el caso de la amina secundaria, los impedimentos estéricos debidos a las cadenas que rodean el nitrógeno dificultan las interacciones entre moléculas. Las aminas con menos de siete carbonos son solubles en agua.  |
PROPIEDADES ÁCIDO-BASE DE LAS AMINAS
Las aminas presentan hidrógenos ácidos en el grupo amino. Estos hidrógenos se pueden sustraer empleando bases fuertes (organometálicos, hidruros metálicos) formando los amiduros (bases de las aminas).
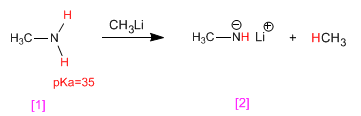
La metilamina [1] reacciona con metillitio, transformándose en su base conjugada, el metilamiduro de litio[2]. Por su parte, el metillitio se transforma en su ácido conjugado, el metano.
La desprotonación de la diisopropilamina produce una de las bases más utilizadas en química orgánica, el diisopropilamiduro de litio (LDA).
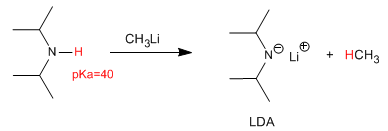
Sin embargo, el comportamiento más importante de las aminas es el básico. Las aminas son las sustancias orgánicas neutras de mayor basicidad.
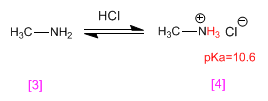
La metilamina [3] se protona transformándose en el cloruro de metilamonio (sal de amonio) [4]. Las sales de amonio son los ácidos conjugados de las aminas y tienen pKas que varían entre 9 y 11.
La basicidad de las aminas depende de los efectos inductivo y estérico. Así, el pKa sube con la longitud de la cadena carbonada (efecto inductivo)
CH3NH2 pKa=10.6
CH3CH2NH2 pKa=10.8
(CH3)3CNH2 pKa=10.4
La cadena carbonada cede carga al grupo amino, por efecto inductivo, aumentando su basicidad. La base fuerte tiene un ácido conjugado debil, por tanto el pKa sube. Pero si la cadena es muy voluminosa, comienzan a predominar efectos estéricos, que provocan una disminución del pKa.
SOLUBILIDAD:Las aminas primarias y secundarias son compuestos polares, capaces de formar puentes de hidrógeno entre sí y con el agua, esto las hace solubles en ella. La solubilidad disminuye en las moléculas con más de 6 átomos de carbono y en las que poseen el anillo aromático.
PUNTO DE EBULLICIÓN: El punto de ebullición de las aminas es más alto que el de los compuestos apolares que presentan el mismo peso molecular de las aminas. El nitrógeno es menos electronegativo que el oxígeno, esto hace que los puentes de hidrógeno entre las aminas se den en menor grado que en los alcoholes. Esto hace que el punto de ebullición de las aminas sea más bajo que el de los alcoholes del mismo peso molecular.

PROPIEDADES QUÍMICAS: Las aminas se comportan como bases. Cuando una amina se disuelve en agua, acepta un protón formando un ión alquil-amonio.
Estructura y enlaces de la Aminas:
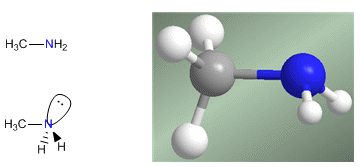
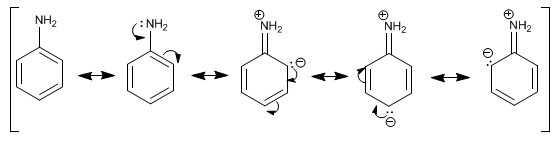
En las aminas aromáticas, como la anilina, la característica más destacable es la deslocalización del par libre en el anillo aromático. Esta deslocalización produce un aumento en la densidad electrónica del grupo fenilo, aumentando la reactividad de la anilina en reacciones de sustitución electrófila.
Síntesis de Aminas:
Las aminas se pueden preparar mediente reacciones de sustitución nucleófila entre haloalcanos y amoniaco.
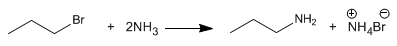
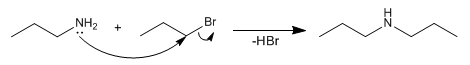
Síntesis de aminas por reducción de nitrilos:
El primer equivalente de amoniaco actúa como nucleófilo, sustituyendo al bromo. El segundo equivalente actúa como base desprotonando la amina.
La amina formada, al igual que el amoniaco, es nucleófila y tiende a reaccionar con el haloalcano que queda libre en el medio, formándose aminas secundarias y terciarias. Este problema hace que el método sea poco útil, debido a la mezcla final obtenida.
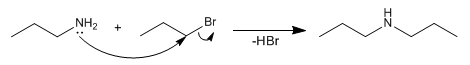
La amina formada vuelve a reaccionar con el haloalcano, alquilándose una segunda vez. Este problema recibe el nombre de polialquilaciones.
Los nitrilos se pueden preparar por reacción de haloalcanos con cianuro de sodio. La reducción de nitrilos con LiAlH4 produce aminas.
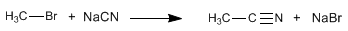
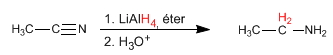
Paso 1. Obtención del nitrilo a partir de haloalcanos primarios o secundarios.
Paso 2. Reducción del nitrilo a amina
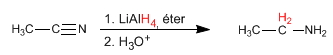
Obsérvese que la amina final tiene un carbono más que el haloalcano de partida.
Nomenclatura de las Aminas:
Regla 1. Las aminas se pueden nombrar como derivados de alquilaminas o alcanoaminas. Veamos algunos ejemplos.

Regla 2. Si un radical está repetido varias veces, se indica con los prefijos di-, tri-,...
Si la amina lleva radicales diferentes, se nombran alfabéticamente.

Regla 3. Los sustituyentes unidos directamente al nitrógeno llevan el localizador N. Si en la molécula hay dos grupos amino sustituidos se emplea N,N'.

Regla 4. Cuando la amina no es el grupo funcional pasa a nombrarse como amino-. La mayor parte de los grupos funcionales tienen prioridad sobre la amina (ácidos y derivados, carbonilos, alcoholes)


Regla 2. Si un radical está repetido varias veces, se indica con los prefijos di-, tri-,...
Si la amina lleva radicales diferentes, se nombran alfabéticamente.

Regla 3. Los sustituyentes unidos directamente al nitrógeno llevan el localizador N. Si en la molécula hay dos grupos amino sustituidos se emplea N,N'.

Regla 4. Cuando la amina no es el grupo funcional pasa a nombrarse como amino-. La mayor parte de los grupos funcionales tienen prioridad sobre la amina (ácidos y derivados, carbonilos, alcoholes)

Clases de Aminas:
- En cuanto a las aminas primarias: las aminas alifáticas (link con Nomenclatura Orgánica cuarta etapa) reaccionan con el ácido nitroso para dar un alcohol con desprendimiento de nitrógeno y agua
- Las aminas aromáticas al reaccionar con ácido nitroso a temperatura elevada en presencia de ácido sulfúrico diluido se comportan como las aminas alifáticas, pero si la reacción ocurre a 0ºC se produce una sal de diazonio soluble en agua.
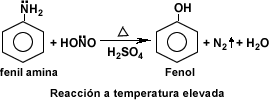
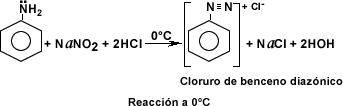
- Las aminas secundarias tanto alifáticas como aromáticas al reaccionar con el ácido nitroso generan N-nitrosaminas oleosas e insolubles en agua, llamadas también compuestos N-nitrosos.
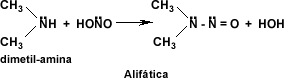
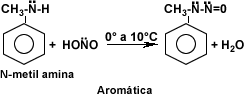
- En cuanto a las aminas terciarias tanto alifáticas como aromáticas al reaccionar con el ácido nitroso generan derivados N-nitrosados y productos complejos respectivamente que son motivo de estudio.
REACCIONES GENERALES DE LAS AMINAS:
Las aminas reaccionan con los ácidos carboxílicos (COOH) para formar las amidas (CONH2), esto ocurre para crear polímeros, en la síntesis de aminoácidos (en la cual el enlace entre ácido y amina se denomina enlace peptídico), y en otros ámbitos.
Reaccionan liberan una molécula de agua:
COOH + H2N ----> CONH2 + H2O
Reaccionan liberan una molécula de agua:
COOH + H2N ----> CONH2 + H2O
Ejemplo:

Reacción de ésteres con aminas
Los ésteres reaccionan con aminas formando amidas, la reacción requiere calefacción.

- Las alquilaciones de las aminas primarias y secundarias dan frecuentemente mezclas de productos. Las aminas terciarias se alquilan dando sales cuaternarias de amonio.
- Las aminas primarias y secundarias se pueden acilar al reaccionar con cloruros de ácido o con anhídridos de ácido, para dar amidas.
Eliminación de Hofmann:
Las aminas se pueden convertir en alquenos mediante una reacción de eliminación. Debido a que el ión amididuro, NH2-, ha de convertirse en un mejor grupo saliente. En la reacción de eliminación de Hofmann, se metila una amina mediante una reacción con exceso de yodometano para producir una sal cuaternaria de amonio, la cual experimenta una eliminación pque da lugar a un alqueno por calentamiento con óxido de plata como base.
Las aminas se pueden convertir en alquenos mediante una reacción de eliminación. Debido a que el ión amididuro, NH2-, ha de convertirse en un mejor grupo saliente. En la reacción de eliminación de Hofmann, se metila una amina mediante una reacción con exceso de yodometano para producir una sal cuaternaria de amonio, la cual experimenta una eliminación pque da lugar a un alqueno por calentamiento con óxido de plata como base.

El óxido de plata actúa intercambiando el ión yoduro por el ión hidróxido en la sal cuaternaria, lo que da la base se necesita para la eliminación.

AMONIÓLISIS Y ALQUILACIÓN DE AMINAS:
En esta reacción, el alcohol pierde el OH y un hidrógeno del amonio se juntan para formar agua, y lo que queda se junta para formar una amina primaria. En la segunda reacción la amina primaria pierde un hidrogeno junta al nitrógeno y el halogenuro pierde el cloro y estos se juntan para formar ácido clorhídrico, y el metilo se junta con la amina para formar una amina secundaria. En la tercera reacción, la amina secundaria pierde el hidrógeno que esta pegado al nitrógeno y se junta con el cloro que pierde el halogenuro para formar ácido clorhídrico y el metilo se pega al nitrógeno para formar una amina terciaria.

Fuente industrial de las Aminas:
Algunas de las aminas más sencillas e importantes se preparan a escalaindustrial mediante procesos que no tienen aplicación como métodos delaboratorio. La amina más importante de todas, la anilina, se prepara de varias maneras:
por reducción de nitrobenceno con hierro y ácido clorhídrico, que son reactivos baratos (o bien, por hidrogenación catalítica,)
por tratamiento del clorobenceno con amoniaco

Temperaturas y presiones elevadas, en presencia de un catalizador. Veremos que el segundo proceso es una sustitución nucleofílica aromática. La metilamina, dimetilamina y trimetilamina se sintetizan industrialmente con metanol y amoniaco:
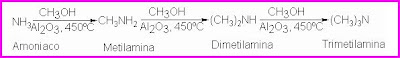
Los halogenuros de alquilo se emplean para hacer algunas alquilaminas superiores, lo mismo que en el laboratorio. Los ácidos obtenidos de lasgrasas.

Pueden convertirse en 1-aminoalcanos de cadena larga con número par de carbonos por la reducción de nitrilos.
Propiedades físicas de las Aminas:
( Acidez, bacidad, obtención).
Propiedades físicas de aminas.
- Son compuestos con geometría piramidal.
- Presentan quiralidad aunque se encuentran en forma de racematos.
- Forman puentes de hidrógeno más débiles que los alcoholes.

- Como bases a través del par libre del nitrógeno.
- Como ácidos débiles pudiendo desprotonarlas mediante el empleo de bases muy fuertes.
- Las aminas se obtienen por reducción de nitrilos y amidas con el hidruro de litio y aluminio.
- La transposición de Hofmann convierte las amidas en aminas con un carbono menos.
- La reducción de azidas permite obtener aminas con el mismo número de carbonos que el haloalcano de partida.
- La síntesis de Gabriel permite obtener aminas a partir del ácido ftálico.
Propiedades físicas de las aminas (2):
Las aminas son compuestos altamente polares. Las aminas primarias y secundarias pueden formar puentes de hidrógeno intramoleculares en el estado líquido y, por tanto, tienen puntos de ebullición mayores que los alcanos de peso molecular equivalente. Una característica de las aminas de bajo peso molecular es su olor a pescado, que en cierta medida es distintivo.
BASICIDAD DE LAS AMINAS:
La basicidad y la nucleofilicidad de las aminas está dominada por el par de electrones no compartido del nitrógeno, debido a este par, las aminas son compuestos que se comportan como bases y nucleófilos, reaccionan con ácido para formar sales ácido/base, y reaccionan con electrófilos en muchas de las reacciones polares.
- Sales de aminas (sales de amonio):
 La diferencia en el comportamiento de las aminas y sus sales, en cuanto a solubilidad, puede utilizarse tanto para detectar aminas como para separarlas de sustancias no básicas. Un compuesto orgánico insoluble en agua que se disuelve en ácido clorhídrico acuoso diluido, debe ser apreciablemente básico, lo que significa que se trata de una amina. Ésta puede separarse de compuestos no básicos por su solubilidad en ácidos; una vez separada, puede regenerarse alcalinizando la solución acuosa.
La diferencia en el comportamiento de las aminas y sus sales, en cuanto a solubilidad, puede utilizarse tanto para detectar aminas como para separarlas de sustancias no básicas. Un compuesto orgánico insoluble en agua que se disuelve en ácido clorhídrico acuoso diluido, debe ser apreciablemente básico, lo que significa que se trata de una amina. Ésta puede separarse de compuestos no básicos por su solubilidad en ácidos; una vez separada, puede regenerarse alcalinizando la solución acuosa.
Uso industrial Aminas:

 Estos compuestos tienen aplicaciones muy diversas de interés industrial: son bactericidas y alguicidas de gran consumo y se utilizan como inhibidores de la corrección de tuberías metálicas o en los líquidos ácidos para limpiar la herrumbre, porque forman una capa hidrófoba protectora al unirse a la superficie del metal por la parte polar.
Estos compuestos tienen aplicaciones muy diversas de interés industrial: son bactericidas y alguicidas de gran consumo y se utilizan como inhibidores de la corrección de tuberías metálicas o en los líquidos ácidos para limpiar la herrumbre, porque forman una capa hidrófoba protectora al unirse a la superficie del metal por la parte polar.Los tenso actínidos catiónicos son agentes de flotación que se utilizan para separar minerales valiosos de su ganga, porque se absorben sobre las partículas cristalinas ácidas. En otros casos el que flota es preferentemente el mineral valioso, dependiendo de su composición.
Los compuestos de tipo b) con dos cadenas largas en el N, son los componentes activos de los productos suavizantes o ablandadores de tejidos que se usan después de el lavado y enjuagado de toallas, sabanas y prendas de vestir al fijarse sobre las fibras por su parte ionica las lubrica e impide su adherencia al secarse.
Las aminas de tipo e) se utilizan para preparar emulsiones de asfalto que se adhieren muy bien al lecho de roca o piedras y al cemento.
Las etanolaminas se utilizan para preparan amidas que son detergentes no iónicos empleados en preparados cosméticos, por su carácter suavizante, y para la fabricación de morfolina, un disolvente industrial de amplio uso.
Bibliografías:
- http://es.answers.yahoo.com/question/index?qid=20071207203014AA48h7t
- http://www.google.com.co/imgres?q=Aminas+uso+industrial&um=1&hl=es&sa=N&biw=1024&bih=499&tbm=isch&tbnid=3A_l2SCZt42vwM:&imgrefurl=http://academic.scranton.edu/faculty/cannm1/advancedorganic/advancedorganicmodulespan.html&docid=4fJ9bxg0hyoCgM&imgurl=http://academic.scranton.edu/faculty/cannm1/advancedorganic/image045.gif&w=574&h=215&ei=az2mTpCLJsTAgQfqqYQj&zoom=1&iact=rc&dur=296&sig=113116068484469851426&page=1&tbnh=69&tbnw=183&start=0&ndsp=9&ved=1t:429,r:3,s:0&tx=130&ty=43
- grupoqo8.blogspot.com/2007/11/aminas-alifticas-usos-riesgos.html
- http://www.google.com.co/search?gcx=c&q=propiedades+aminas&um=1&ie=UTF-8&hl=es&tbm=isch&source=og&sa=N&tab=wi&biw=1024&bih=499
- http://www.google.com.co/imgres?q=Mapa+conceptual+aminas&um=1&hl=es&sa=N&biw=1024&bih=499&tbm=isch&tbnid=DFGaNAuzK4q3XM:&imgrefurl=http://chicasingadministradoras.blogspot.com/&docid=_hy2Jd7C7Ll7QM&imgurl=https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEh1LoxIPXRTR2rC8Rkm3ReEYmJ_dF6LwDVZSA3EK3lDOatF58i3K04riy1pe7dYFQKCAmJVkSEBILE7ZVhu6j1pbvJZLh49oKO_ulTyKrbClk_FWDL-mzzhPba9-MpJ7s6SIfoh89LAvCM/s320/comp%252Borga%252B-%252Bcompuestos%252Borganicos.jpg&w=320&h=232&ei=5j-mTpLcEYmatweWnvUF&zoom=1&iact=hc&vpx=106&vpy=202&dur=75&hovh=185&hovw=256&tx=137&ty=167&sig=113116068484469851426&page=4&tbnh=124&tbnw=171&start=29&ndsp=9&ved=1t:429,r:5,s:29
- http://www.google.com.co/imgres?q=Aminas&um=1&hl=es&sa=N&biw=1024&bih=499&tbm=isch&tbnid=esK0JJk1mN3ODM:&imgrefurl=http://www.monografias.com/trabajos16/derivados-petroleo/derivados-petroleo.shtml&docid=4TYWO6CTdpcgCM&imgurl=http://www.monografias.com/trabajos16/derivados-petroleo/Image5434.gif&w=509&h=465&ei=1jimTqziOsG1twe4negU&zoom=1&iact=hc&vpx=590&vpy=171&dur=2148&hovh=215&hovw=235&tx=30&ty=142&sig=113116068484469851426&page=1&tbnh=126&tbnw=138&start=0&ndsp=10&ved=1t:429,r:3,s:0
- http://www.ulpgc.es/descargadirecta.php?codigo_archivo=4543
- http://patentados.com/img/2004/aminas-biciclicas-como-insecticidas.png
- http://www.google.com.co/search?gcx=c&q=polaridad&um=1&ie=UTF-8&hl=es&tbm=isch&source=og&sa=N&tab=wi&biw=1024&bih=499



